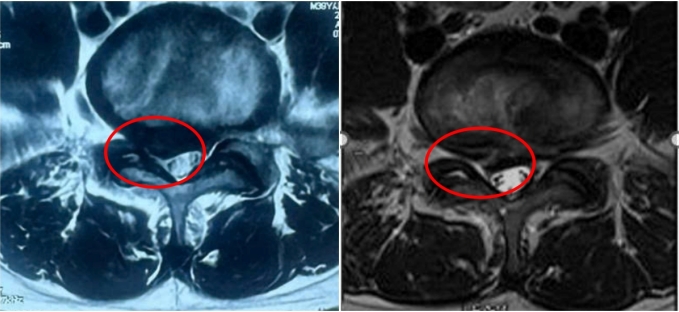
Cục Quản lý Dược đã ra quyết định thu hồi thuốc Femancia (số đăng ký VD-27929-17) do Công ty Cổ phần Dược phẩm MeDiSun (TP.HCM) đăng ký, kể từ ngày 17/7.
Lý do thu hồi là vì thuốc Femancia đã có hai lô vi phạm chất lượng ở mức độ 2 trong vòng 60 tháng. Theo quy định của Luật Dược, giấy đăng ký lưu hành thuốc sẽ bị thu hồi nếu có ít nhất hai lô thuốc bị thu hồi bắt buộc do vi phạm mức độ 2 trong vòng 5 năm kể từ ngày được cấp phép.
Vi phạm chất lượng thuốc được phân loại theo ba mức độ khác nhau. Mức độ 2 chỉ những vi phạm khi thuốc không đạt tiêu chuẩn về các chỉ tiêu không định tính và không trực tiếp gây nguy hiểm nghiêm trọng cho sức khỏe hoặc tính mạng người sử dụng. Tuy nhiên, vi phạm này có thể ảnh hưởng đến hiệu quả điều trị hoặc gây ra những rủi ro an toàn nếu sử dụng thuốc trong thời gian dài hoặc với liều lượng cao. Các chỉ tiêu thường gặp trong vi phạm mức độ 2 bao gồm độ hòa tan, định lượng và độ ổn định của thuốc.
Quyết định này đồng nghĩa với việc Femancia sẽ không được phép sản xuất và lưu hành trên thị trường Việt Nam. Công ty Cổ phần Dược phẩm MeDiSun có trách nhiệm phải tiến hành thu hồi toàn bộ số thuốc Femancia hiện có trên thị trường theo đúng quy định của pháp luật.

Trước đó, vào tháng 3, Cục Quản lý Dược cũng đã thông báo thu hồi hai lô thuốc viên nang cứng Femancia (chứa Sắt fumarat 305mg tương đương Sắt nguyên tố 100mg và Acid Folic 350mcg, số đăng ký VD-27929-17). Nguyên nhân thu hồi là do hai lô thuốc này không đạt tiêu chuẩn chất lượng về chỉ tiêu định lượng và độ hòa tan, vi phạm mức độ 2.
Theo thông tin trên các trang web của các trung tâm thuốc, Femancia được biết đến là một loại thuốc bổ sung sắt, có tác dụng ngăn ngừa tình trạng thiếu máu và thiếu sắt.
Admin
Nguồn: VnExpress